Por segunda vez, los investigadores del cáncer de la Universdidad de Vanderbilt (Nashville, Tennessee) han descubierto una proteína que, cuando se manipula genéticamente para impedir que interactúe con un gen responsable de la génesis del cáncer, deshace los tumores de manera efectiva en días. El artículo se titula «MYC regula la biogénesis de ribosomas y los programas de expresión de genes mitocondriales a través de la interacción con Host Cell Factor-1 (HCF1)».
Los tumores se forman cuando las células pierden el control de su crecimiento. Por lo general, las células producen señales que controlan cuánto y con qué frecuencia se dividen. Pero si estas señales se vuelven defectuosas, las células pueden crecer demasiado rápido o multiplicarse con demasiada frecuencia. Por ejemplo, un grupo de proteínas conocidas como proteínas MYC activan los genes de crecimiento en una célula, pero demasiadas de estas proteínas hacen que las células crezcan de manera incontrolable.
Con un tercio de todas las muertes por cáncer relacionadas con el exceso de proteínas MYC, estas moléculas podrían ser objetivos clave para los medicamentos contra el cáncer. Sin embargo, los tratamientos actuales no se dirigen a estas proteínas. Una opción para tratar los cánceres relacionados con las proteínas MYC podría ser apuntar a proteínas que funcionan junto con las proteínas MYC, como la proteína HCF1, que puede unirse a las proteínas MYC.
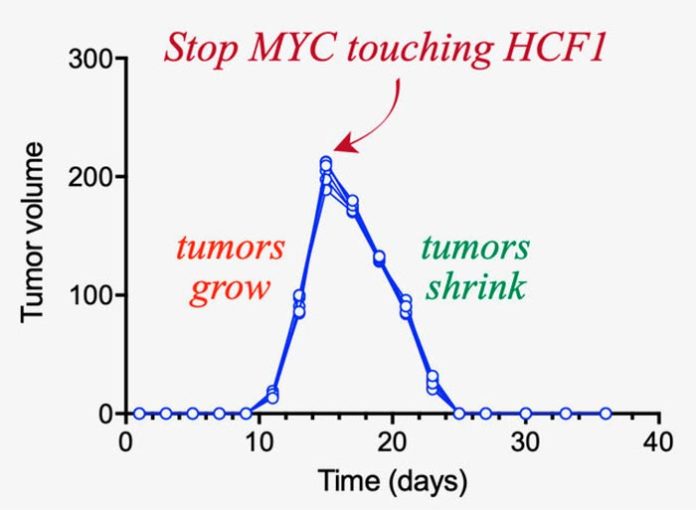
Para probar si el HCF-1 podría ser un objetivo farmacológico potencial, el equipo de investigadores estudió cómo interactuaban las proteínas HCF1 y MYC utilizando células cancerosas específicas cultivadas en el laboratorio. Esto reveló que cuando las dos proteínas se conectaron, activaron genes que desencadenan un rápido crecimiento celular. Cuando estas células cancerosas se inyectaron en ratones, los tumores crecieron rápidamente. Sin embargo, cuando se interrumpieron las uniones de MYC y HCF1 en las células cancerosas, los tumores se redujeron. Esto sugiere que si los medicamentos contra el cáncer pudieran apuntar a las proteínas HCF1, podrían potencialmente reducir o incluso revertir el crecimiento de tumores.
La HCF1 es afectada por MYC y es importante para estimular la síntesis de proteínas
William Tansey, profesor de biología y bioquímica celular y del desarrollo, se dedica a comprender cómo funciona la familia de oncogenes MYC (L-myc, N-myc y c-myc), que codifican proteínas. La proteína MYC, similar a un fideo, altamente conservada, realiza funciones importantes en el desarrollo humano normal y, a menudo, se reactiva en los cánceres más mortíferos y difíciles de tratar.
«MYC impulsa rondas implacables de duplicación y división celular«, comenta Tansey. «Cuanto más rápido crecen y se dividen las células, acumulan mutaciones que dan lugar al crecimiento del cáncer«.
MYC ha sido un objetivo de terapias difícil de alcanzar durante al menos 30 años, según Tansey, y se ha considerado imposible de transformar en medicamento debido a su falta de estructura. Para solucionar este obstáculo, Tansey se propuso identificar las proteínas asociadas más estructuradas de MYC con el objetivo de diseñar mutaciones que interrumpan las interacciones de los socios con MYC que causan el crecimiento del cáncer. «Si podemos validar el contacto físico entre MYC y una proteína, podemos localizarla de forma terapéutica«.
Tansey y sus colaboradores han identificado la proteína Host Cell Factor-1 como una candidata definitiva para este tipo de desarrollo terapéutico. La HCF1 es afectada por MYC y es importante para estimular la síntesis de proteínas. Cuando una célula cancerosa con MYC se modifica genéticamente para que ya no interactúe con HCF1, la célula cancerosa comienza a autodestruirse. Desarrollar una terapia que limite esta interacción es un paso muy prometedor en el tratamiento del cáncer.
«Lo interesante es que no es necesario eliminar todas las funciones de MYC«, afirma Tansey. «Como un talón de Aquiles, sólo necesitamos buscar una interacción muy específica«.
Esta es la segunda proteína descubierta por Tansey que responde a MYC de esta manera. Un descubrimiento anterior de la proteína WDR5 en colaboración con Stephen Fesik, profesor de Investigación del Cáncer en Orrin H. Ingram II, mostró un comportamiento muy similar. Ambas proteínas se escondían a plena vista.
«MYC se une físicamente al ADN para activar genes. Los factores de transcripción de proteínas sólo necesitan dos dominios: un dominio de unión al ADN y un dominio de activación que estimula al ADN a producir ARN y proteínas. Estamos interesados en el bit intermedio, la pieza huérfana de la proteína que nadie más había examinado seriamente«, concluye Tansey.
Como resultado de cuatro años de trabajo riguroso, el laboratorio de Tansey tiene la intención de disponer de una mejor idea de cómo funciona HCF1 con MYC y cómo afecta otras funciones de las proteínas.
Fuente: eLife Sciences.

























