Las enfermedades neurodegenerativas como la enfermedad de Alzheimer o la enfermedad de Parkinson están causadas por errores de plegamiento en proteínas o péptidos, es decir, por cambios en su estructura espacial. Este es el resultado de diminutas desviaciones en la composición química de las biomoléculas. Investigadores del Instituto de Tecnología de Karlsruhe (KIT) han desarrollado un método simple y efectivo para detectar dicho mal plegamiento en una etapa temprana de la enfermedad.
El mal plegamiento se revela por la estructura del residuo seco de las soluciones de proteínas y péptidos. El método consiste en analizar micrografías con redes neuronales y tiene una precisión predictiva de más del 99 %. Los resultados han sido publicados en Advanced Materials.
«Los patrones de tinción de los péptidos beta amiloides sirven como huellas dactilares exactas para detectar el Alzheimer que reflejan la identidad estructural y espacial de un péptido«
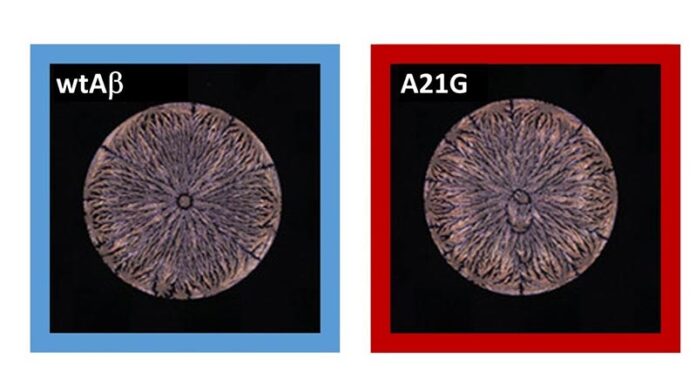
La estructura bioquímica de proteínas y péptidos determina sus funciones biológicas. Hay muchos indicios de que incluso los cambios estructurales o espaciales más pequeños pueden promover el desarrollo de enfermedades. Muchas enfermedades neurodegenerativas se han atribuido al mal plegamiento de proteínas y péptidos causado por dichos cambios. Los péptidos beta amiloide (Aβ42) juegan un papel clave en la enfermedad de Alzheimer; difieren en un solo residuo de aminoácido y representan mutantes hereditarios de la enfermedad de Alzheimer.
Hasta ahora no había un método simple y preciso para predecir mutaciones en proteínas. En el Instituto de Interfaces Funcionales (IFG) de KIT, un grupo de investigación dirigido por el profesor Jörg Lahann ha desarrollado un método para detectar el plegamiento incorrecto a través de la estructura de soluciones de péptidos y proteínas secas. «Los patrones de tinción no solo fueron característicos y reproducibles, sino que también dieron como resultado una clasificación de ocho mutaciones con una precisión predictiva de más del 99 %», comenta Lahann, autor del estudio, al describir los resultados. El grupo demostró que se puede obtener información crucial sobre las estructuras primaria y secundaria de los péptidos a partir de las manchas que quedan al secar gotas de solución peptídica sobre una superficie sólida.
Patrones de tinción como huellas dactilares peptídicas exactas
Las soluciones de proteínas y péptidos se colocan con precisión en portaobjetos de vidrio mediante un sistema de pipeteo automático para garantizar resultados controlados y reproducibles. Las superficies de los portaobjetos se prepararon previamente con un revestimiento de polímero hidrofóbico. Para analizar los complejos patrones de tinción de las gotas secas, los investigadores adquirieron imágenes mediante microscopía de polarización. Luego, las imágenes se analizaron con redes neuronales de aprendizaje profundo.
«Dado que las estructuras son muy similares y difíciles de distinguir a simple vista, definitivamente fue una sorpresa que las redes neuronales fueran tan efectivas», indica Lahann sobre los resultados. «Los patrones de tinción de los péptidos beta amiloides sirven como huellas dactilares exactas que reflejan la identidad estructural y espacial de un péptido». Esta tecnología permite la identificación de variantes de Alzheimer con máxima resolución en pocos minutos, según Lahann.
La preparación simple de muestras brinda diagnósticos rápidos
Los resultados sugieren que un método tan simple como secar una gota de solución peptídica sobre una superficie sólida puede servir como indicador de diferencias mínimas en las estructuras primaria y secundaria de los péptidos. «Se necesitan urgentemente métodos de detección escalables y precisos para la estratificación de alteraciones de proteínas estructurales y conformacionales para decodificar las firmas patológicas de enfermedades como el Alzheimer y el Parkinson», asegura Lahann.
También es un método relativamente simple que no requiere una preparación elaborada de muestras y, por lo tanto, permite un diagnóstico simple y fácil para el paciente. Además, el método tiene un gran potencial para otras aplicaciones en el diagnóstico médico y en la detección molecular de enfermedades.
Fuente: Advanced Materials.
























