El cáncer de ovario es la quinta causa principal de muerte por cáncer entre las mujeres, y es tan mortal, en parte, porque la enfermedad es difícil de detectar en sus primeras etapas. Las pacientes a menudo no experimentan síntomas hasta que el cáncer ha comenzado a propagarse y no existen pruebas de detección confiables para la detección temprana.
Un equipo de investigadores está trabajando para cambiar eso. El grupo incluye investigadores del Centro de Cáncer Memorial Sloan Kettering, Weill Cornell Medicine, la Universidad de Maryland, los Institutos Nacionales de Estándares y Tecnología de EE.UU. y la Universidad de Lehigh.
«Es como tener 20 pares de ojos que ven cosas superpuestas. Ningún ojo es tan bueno, pero como grupo, se pueden entrenar para que funcionen mejor que los métodos de detección existentes para el cáncer de ovario«
Dos artículos recientes describen sus avances hacia un nuevo método de detección del cáncer de ovario. El enfoque utiliza técnicas de aprendizaje automático para analizar de manera eficiente las firmas espectrales de los nanotubos de carbono para detectar biomarcadores de la enfermedad y reconocer el cáncer en sí.
El primer artículo apareció en Science Advances en noviembre.
«Demostramos que una plataforma de nanosensores basada en la percepción podría detectar biomarcadores de cáncer de ovario mediante el aprendizaje automático«, afirma Yoona Yang, investigadora asociada postdoctoral en el Departamento de Ingeniería Química y Biomolecular de Lehigh y coprimera autora del artículo junto con Zvi Yaari, investigadora postdoctoral investigadora del Memorial Sloan Kettering Cancer Center en Nueva York. Los autores también incluyeron a Ming Zheng, químico investigador del Instituto Nacional de Estándares y Tecnología, Anand Jagota, profesor de bioingeniería e ingeniería química y biomolecular en la Universidad de Lehigh, y Daniel Heller, miembro asociado y director del Laboratorio de Nanotecnología del Cáncer en el Memorial Centro Oncológico Sloan Kettering.
En esta enfermedad no hay un solo biomarcador
Jagota, quien también se desempeña como decano asociado de investigación de la Facultad de Salud de Lehigh, y Yang son miembros de Nano | Iniciativa Presidencial de Interfaces Humanas, una iniciativa de investigación multidisciplinaria que tiene como objetivo cambiar la forma en que trabajamos con datos y los instrumentos sofisticados del descubrimiento científico.
Tradicionalmente, la detección de biomarcadores de enfermedades requiere que una molécula de reconocimiento molecular, como un anticuerpo, coincida con cada marcador. Pero para el cáncer de ovario, no hay un solo biomarcador, o analito, que indique la presencia de cáncer. Cuando es necesario medir múltiples analitos en una muestra determinada, lo que puede aumentar la precisión de una prueba, se requieren más anticuerpos, lo que aumenta el coste de la prueba y el tiempo de respuesta.
La percepción del cerebro humano, clave en la idea
«Funciones de detección basadas en una percepción como la del cerebro humano«, indica Yang. «El sistema consiste en una matriz de detección que captura una determinada característica de los analitos de una manera específica, y luego la respuesta del conjunto de la matriz es analizada por el modelo perceptivo computacional. Puede detectar varios analitos a la vez, lo que lo hace mucho más eficiente.»
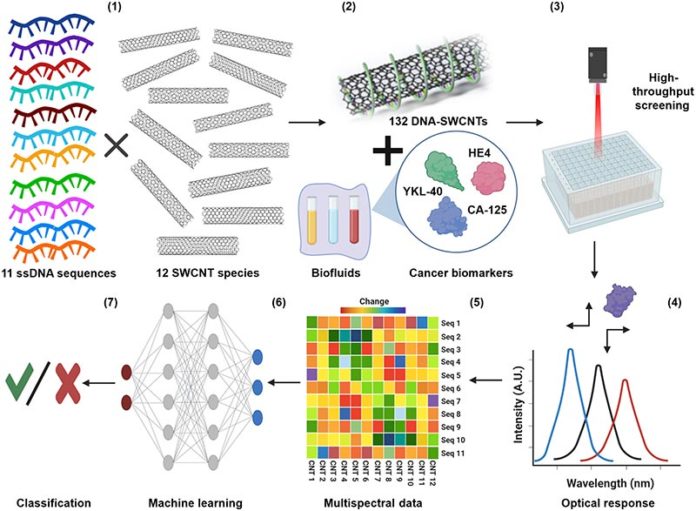
Para este estudio en particular, la matriz constaba de nanotubos de carbono de pared simple envueltos en hebras de ADN. La forma en que se envolvió el ADN y la variedad de secuencias de ADN que se utilizaron crearon una diversidad de superficies en los nanotubos. Las diversas superficies, a su vez, atrajeron una variedad de proteínas dentro de una muestra de lavado uterino enriquecida con niveles variables de biomarcadores de cáncer de ovario.
Sensores no específicos
«Los nanotubos de carbono tienen propiedades electrónicas interesantes«, afirma Heller. «Si les disparas luz, emiten un color de luz diferente, y el color y la intensidad de esa luz pueden cambiar en función de lo que se adhiera al nanotubo. Pudimos aprovechar la complejidad de tantas interacciones de unión potenciales mediante el uso de una gama de nanotubos con varios envoltorios. Y eso nos dio una gama de diferentes sensores que podían detectar cosas ligeramente diferentes, y resultó que respondían de manera diferente a distintas proteínas«.
El algoritmo de aprendizaje automático se entrenó utilizando los datos de la emisión de nanotubos, las firmas espectrales, para reconocer el patrón de emisión que indicaba la presencia y concentración de cada biomarcador.
«El avance conceptual aquí es que estos nanotubos son sensores no específicos«, indica Jagota. «No saben nada sobre biomarcadores, lo que significa que no están programados para unirse a nada específico. Todo lo que sabíamos es que pueden estar expuestos a un medio acuoso, y cualquier cosa a la que estén expuestos dentro de ese medio producirá cambios espectrales y de magnitud. Y usando una combinación de estos sensores, pudimos entrenar el algoritmo para transformar matemáticamente estas entradas en salidas con alta precisión. Es como tener 20 pares de ojos que ven cosas superpuestas. Ningún ojo es tan bueno, pero como grupo, se pueden entrenar para que funcionen mejor que los métodos de detección existentes para el cáncer de ovario«.
En busca de la enfermedad, no de los biomarcadores
El segundo artículo apareció en marzo en Nature Biomedical Engineering y comprendía el trabajo de muchos de los mismos investigadores. Además, los autores incluyeron a YuHuang Wang, profesor en el departamento de química y bioquímica de la Universidad de Maryland, y Mijin Kim, investigadora asociada postdoctoral en Memorial Sloan Kettering Cancer Center, quien fue la autora principal del estudio.
«En este documento, ya no buscábamos biomarcadores, buscábamos la enfermedad en sí«, recuerda Heller. «Queríamos saber, ¿podría esta tecnología diferenciar una muestra de sangre de una paciente con cáncer de ovario de una paciente sin él?»
Nanotubos con defectos cuánticos
Esos pacientes sin cáncer de ovario incluían tanto a personas sanas como a personas con otras enfermedades. En este estudio, los nanotubos fueron dotados con defectos cuánticos, lo que esencialmente aumentó la diversidad de respuestas que proporcionarían los nanotubos.
«Los nanotubos tenían una determinada molécula unida que les daba una señal adicional en términos de datos«, comenta Jagota. «Entonces, datos más ricos provinieron de cada combinación de nanotubos y ADN. Y el modelo no se entrenó en el biomarcador, sino en el estado de la enfermedad«.
La huella dactilar de la enfermedad
El modelo desarrolló una «huella dactilar de la enfermedad» a partir de las emisiones espectrales de los nanotubos. Los resultados fueron estadísticamente significativos en cuanto a la especificidad del modelo en la detección del cáncer de ovario y la sensibilidad en la detección de biomarcadores conocidos y desconocidos de la enfermedad.
Heller afirma que una analogía de cómo funciona el modelo de aprendizaje automático, en ambos artículos, es la nariz humana. Por ejemplo, no hay un solo receptor de olor para cada olor.
«En cambio, hay un montón de diferentes receptores de olores que se unen a ciertas moléculas y crean un patrón o una especie de huella digital«, asegura. «Y ese patrón es procesado por tu cerebro, que a su vez te dice lo que estás oliendo. Así que aquí no hay un sensor en particular que responda a una cosa en particular. Pero, según el patrón de diferentes sensores que responden con varios cambios en color e intensidad de longitud de onda, el algoritmo puede interpretar qué es un biomarcador y qué no, o qué es una enfermedad y qué no lo es«.
Aún falta identificar las primeras etapas de la enfermedad
El equipo ha demostrado que su técnica puede detectar el cáncer de ovario mejor que los métodos actuales, pero aún no puede identificar las primeras etapas de la enfermedad. En parte, según Heller, el problema es encontrar suficientes muestras para entrenar el algoritmo porque muy pocas personas son diagnosticadas en esos momentos.
«Estamos trabajando para determinar cómo podemos detectar esta enfermedad en las etapas más tempranas posibles«, indica. Los próximos pasos también podrían incluir expandirse para desarrollar la técnica para una variedad de enfermedades y determinar si se puede optimizar para que funcione en condiciones clínicas, comenta Jagota.
«Y esta es una técnica que se puede aplicar en una variedad de áreas«, según Jagota. «Nos enfocamos en la salud, pero podría usarse para identificar contaminantes en el aire, por ejemplo. Existe el potencial de atacar muchas enfermedades y condiciones diferentes, y eso me parece fascinante«.
Fuentes: Science Advances y Nature Biomedical Engineering.

























