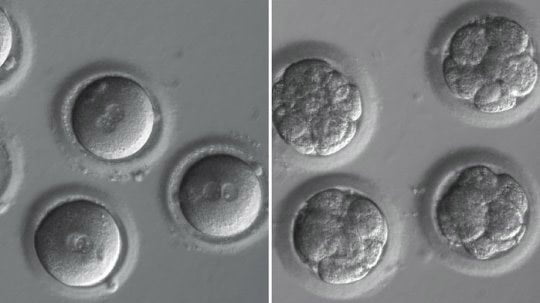
La utilización clínica de la técnica CRISPR para editar ADN y alterar embriones humanos es a partir de hoy menos hipotética. Un equipo de investigadores ha publicado por primera vez la demostración rigurosa de que esta técnica puede reparar de forma eficiente un defecto genético en embriones humanos –que podría causar un potencial fallo cardíaco letal- sin introducir nuevas mutaciones.
Aunque ninguno de estos embriones de laboratorio fueron transferidos a mujeres, el equipo de investigación, liderado por el biólogo estadounidense Shoukhrat Mitalipov, especialista en embriones de la Oregon Health and Science University (OHSU) en Portland, afirma que este éxito pone las bases para utilizar la técnica en la prevención clínica de la transmisión de enfermedades genéticas.
Según los investigadores, CRISPR es eficiente a la hora de rescatar embriones mutados que de otro modo serían eliminados en los procedimientos de fertilización in vitro. Pero la seguridad a largo plazo de la técnica aún no es clara, y muchos investigadores han argumentado que la edición de rasgos permanentes y heredables del ADN pueden corregir enfermedades genéticas, pero también introducir otros rasgos de diseño.
El laboratorio de Mitalipov exploró una técnica para prevenir la transmisión de mutaciones causantes de enfermedades en las mitocondrias de una mujer -orgánulos celulares con sus propios genes- transfiriendo su ADN nuclear en un óvulo donado, algo controvertido porque cualquier descendiente heredaría ADN de tres individuos.
Pero el proyecto de edición de ADN CRISPR fue particularmente difícil de vender a la universidad, según Mitalipov. Primero hizo una propuesta a la OHSU hace tres años. Su plan era utilizar CRISPR —una enzima de corte de ADN y ARN que lo guía a una secuencia diana- para cortar el gen MYBPC3 justo en el lugar en el que la mutación conduce al desarrollo de un corazón de mayor tamaño del habitual, y puede ocasionar paro cardíaco incluso en individuos aparentemente sanos y jóvenes. Los investigadores insertarían en su lugar pequeñas secuencias sanas de ADN. Entonces, confiarían en la habilidad natural del ADN para reparar estos cortes, esperando que utilice la secuencia sana como muestra.
La universidad nombró dos comités para juzgar esta propuesta; una se encargaría del aspecto científico y otra del ético. Algunos de sus miembros dudaron mucho a la hora de firmar la propuesta favorablemente. Los otros tres estudios previos sobre edición de ADN en embriones, todos chinos, habían sugerido que la enzima CRISPR a veces corta trozos de ADN de forma no intencionada, y también producían embriones mosaico: una porción de sus células contenían el gen saludable, mientras que otros mantenían el mutado. Algunos miembros de los comités de la universidad manifestaron su preocupación sobre estos riesgos, según Mitalipov.
Otros cuestionaron si la tecnología CRISPR era necesaria, ya que una persona con una copia mutada del gen MYBPC3 tiene un 50% de posibilidades de transmitir la copia saludable, y los doctores ya pueden eliminar embriones mutados. Por supuesto, hay personas con dos copias mutadas del gen, pero esta condición es mucho menos habitual). Sin embargo, Mitalipov convenció a los miembros poco dispuestos de ambos comités con un argumento: “Descartar el 50% de embriones por una copia mutada es moralmente cuestionable, cuando disponemos del método para corregir la mutación”.
Aunque finalmente convenció a la universidad, el estudio no podía realizarse con fondos públicos estadounidenses, ya que requería la creación y destrucción de embriones humanos. La OHSU utilizó, pues, fondos institucionales.
El equipo de investigación consiguió óvulos donados de mujeres compensadas económicamente por el esfuerzo, y esperma de un hombre con la copia mutada del gen MYBPC3. En lugar de inyectar CRISPR unas horas tras la fertilización del óvulo, como se hizo en experimentos anteriores, añadieron este sistema junto con el esperma, para prever el efecto mosaico, antes de que el óvulo tuviera oportunidad de dividirse y hacer copias del gen mutado. Y para reducir la oportunidad de cortes no deseados en otras partes del genoma, usaron una versión de CRISPR con vida más corta, cuya enzima y guía ARN no se pega en la célula tras la edición inicial.
De los 58 embriones que se desarrollaron tras la inyección de CRISPR, casi tres cuartas partes pudieron reparar la copia del gen mutado paterno MYBPC3. Ninguno de ellos albergaba células con el gen mutado, y no se encontraron evidencias de cortes en el ADN fuera de la zona diana.
Inesperadamente, todos excepto uno de estos embriones repararon el gen mutado con la copia sana existente (heredada de la donante de óvulos), en lugar de la plantilla añadida.
“El estudio parece aliviar muchas de las preocupaciones sobre los riesgos de esta técnica”, afirma George Daley, investigador de células madre en el Boston Children’s Hospital y decano de la Harvard Medical School en Boston, “pero es muy importante no interpretar ni generalizar”, ya que el riesgo de edición en partes no intencionadas del ADN varía según el gen diana, según él.
A pesar del éxito de este estudio, las implicaciones científicas y éticas aún son objeto de debate. El propio Mitalipov confiesa que es peligroso que la técnica se generalice antes de comprender totalmente las implicaciones hereditarias a largo plazo. Sin embargo, también señala que las clínicas privadas la utilizarán de una forma u otra, incluso sin disponer de un conocimiento completo, así que conviene continuar las investigaciones y eliminar riesgos.
A principios de este año, la U.S. National Academy of Sciences y la National Academy of Medicine en Washington, D.C., adoptaron una posición clara al respecto de esta técnica: el uso clínico de la edición de ADN a este nivel podría permitirse, pero sólo en situaciones en las que una pareja no pudiera tener un hijo sano de otra manera.
¿Variará el criterio más adelante, en función de posteriores estudios?
Fuente: Science.